Центр Избирательной Хронофототерапии Реабилитации и Иммунокоррекции. Москва 2021 г.
врач онколог к.м.н. Пащенко Наталья Владимировна,
Избирательная Хронофототерапия – новый метод поддерживающей терапии в онкологической практике.
В настоящее время генеральной концепцией клинической и экспериментальной онкологии при лечении злокачественных опухолей является увеличение общей выживаемости (ОВ) и качество жизни больного (КЖ). Поддерживающая терапия является основополагающим фактором в достижении этих целей.
Поддерживающая терапия – это профилактика и лечение нежелательных явлений, возникающих в результате злокачественного заболевания или при проведении противоопухолевого лечения. Коррекция нежелательных явлений включает в себя восстановление физических и психологических функций на протяжении всего противоопухолевого лечения, а также в период реабилитации. Интенсивная реабилитация, профилактика рецидива заболевания, увеличение выживаемости и помощь пациентам в терминальной фазе – основные задачи проведения поддерживающей терапии
Международный интерес к проблеме поддерживающей терапии привел к созданию в 1990 г. в Санкт-Галлене Международной ассоциации по поддерживающей терапии в онкологии «MASCC» и журнала «Journal of Supportive Care in Cancer». В работе ассоциации используется опыт не только онкологов, но и специалистов, работающих практически во всех областях медицины. В 2008 г. МАSCC опубликовал официальный термин «supportive care» или “поддерживающая терапия”.
В РФ поддерживающая терапия – важное направление в онкологии, которое развивается весьма активно. Российским обществом клинической онкологии созданы российские практические рекомендации по поддерживающей терапии в онкологии. В 2015 г. Россия вошла в европейскую группу MASCC, а также в состав рабочей группы по поддерживающей терапии и паллиативной помощи общества химиотерапевтов (ESMO) [23; 24].
Основные методы современного противоопухолевого лечения, такие как операционное лечение, химиотерапия, лучевая терапия приводят к угнетению иммунных функций организма. Установлено, что полостная операция по удалению опухоли приводит к подавлению иммунной системы, что выражается в уменьшении количества лимфоцитов и NK – клеток [23; 54]. Угнетение “белого” ростка кроветворения при проведении противоопухолевой химиотерапии и лучевой терапии сопряжено с риском развития инфекционных осложнений, иммуносупрессией, несвоевременному восстановлению показателей крови, что задерживает начало очередного курса лечения и приводит к потере эффективности противоопухолевого лечения.
Метод Избирательной Хронофототерапии (ИХФТ) позволяет путем восстановления иммунного статуса значительно снизить побочные эффекты от стандартного противоопухолевого лечения. В методику входит применение фотодинамической терапии (ФДТ) в сочетании с биохронотерапией. ФДТ терапия включает в себя внутрикожное и внутривенное введение фотосенсибилизатора Хлорин е6 и лазеротерапию. Фотосенсибилизатор (ФС) хлорин Е6 относится к препаратам второго поколения, который проявляет фотодинамический эффект при взаимодействии со светом с длиной волны 660-665 нм. ФС полностью выводится из организма в течение нескольких дней, имеет коэффициент накопления в опухоли (1:10) и практически не обладает фототоксичностью. Лазеротерапия включает в себя использование излучения с длиной волны 662 нм, мощностью 2 Вт., которое проникает в ткани на глубину 20 мм (по нашим данным существенно глубже), что позволяет применять их для опухолей более глубоких локализаций. Лазер оснащен датчиками пульса и дыхания, установленные на теле пациента, что позволяет осуществлять биосинхронизацию лазерного воздействия только в фазах выдоха и диастолы (моменты уменьшения кровенаполнения ткани), что увеличивает глубину проникновения излучения [10; 8].
Уникальный метод биохронотерапии, разработанный и предложенный академиком РАЕН, заведующим лабораторией хронобиологии НИИ физики Ростовского госуниверситета С.Л. Загускиным на основании многолетних исследований и нашедший свое практическое применение в Центре ИХФТ, относятся именно к таким методикам. В основе метода лежит использование индивидуальных биологических ритмов больного в качестве обратной связи при физиотерапевтическом воздействии на пораженный орган или ткань.
Исследования показали, что обменные процессы в клетке, ее энергетика в значительной мере синхронизированы с ритмами пульса и дыхания, что и позволило использовать эти ритмы в качестве обратной связи при создании метода биохронотерапии. Метод биохронотерапии предполагает физиотерапевтическое воздействие на клетки пораженного органа или ткани с целью активизации обменных процессов на клеточном уровне.
Были разработаны и внедрены лазерные приборы, учитывающие индивидуальные биоритмы больного и осуществляющие выбор фазы воздействия автоматически при помощи датчиков дыхания и пульса на теле больного, что служит обратной связью с процессами в клетке, синхронизированными именно с этими ритмами.
Молекулярные механизмы прямого фотодинамического повреждения злокачественных клеток основаны на фотохимических реакциях двух типов [43]. Фотоокисление первого типа включает прямое воздействие возбужденного фотосенсибилизатора (ФС) с субстратом, что приводит к образованию переходных соединений, вступающих в реакцию с кислородом с генерацией его свободных радикалов. В реакциях второго типа происходит перенос энергии от сенсибилизатора, находящегося в возбужденном состоянии, на молекулы кислорода с образованием синглетного кислорода.
Синглетный кислород, в свою очередь, образует нестабильные циклические пероксиды, легко разрушаемые в термических и ферментативных процессах. При этом формируются продукты деструкции субстрата и свободные радикалы [9]. Результатом реакций обоего типа является генерация активных форм кислорода (АФК), таких как синглетный кислород, супероксид-ион и гидроксильный радикал [15; 29]. В последние годы показано, что в каскаде ФДТ – индуцированных биохимических реакций одну из ключевых ролей могут играть окислы азота [39; 48]. Однако преимущественный вклад при ФДТ вносит синглетный кислород.
Образование АФК является неотъемлемым фактором функционирования клеток организма человека и животных. В физиологических условиях образование АФК в клетках сдерживается на низком уровне системой ферментативных и неферментативных антиоксидантов [17]. Вызываемые ФДТ нарушение баланса в системе «АФК-антиоксиданты» и преобладание продукции АФК активацией деструктивных цитотоксических процессов, объединяемых термином «оксидантный стресс». Наработка высокотоксичных АФК является причиной повреждения субклеточных структур и нарушения жизнедеятельности живой клетки, внеклеточных структур и тканей [29]. Интенсивность и характер цитотоксического воздействия зависят от количества генерированных АФК и антиоксидантной активности биологического объекта (рис.1). Критическим фактором, определяющим результат фотодинамического воздействия, является локализация ФС внутри клетки [20; 43; 51; 53]. Непосредственным результатом действия ФДТ на клетку может быть некроз, апоптоз или остановка клеточного цикла с последующим восстановлением нормальной жизнедеятельности. Результатом цитотоксического воздействия ФДТ является уменьшение числа опухолевых клеток.
Другой важный компонент гибели злокачественной опухоли заключается в фотодинамическом воздействии на сосуды опухоли и снижении васкуляризации. Как было показано с помощью флуоресцентных и радиоизотопных методов, во внеклеточном пространстве ФС накапливаются преимущественно в сосудах опухоли и периваскулярной ткани, где индуцируют генерацию высокореакционных АФК [21]. АФК вызывают активацию перекисного окисления липидов мембран и ферментативных систем эндотелия, играющих важную роль в повреждении эндотелиальных и других клеток сосудистой стенки [17]. Фототоксические изменения эндотелия сосудов могут инициировать ряд событий, приводящих к полной окклюзии кровеносных сосудов опухоли [32; 38]. Следствием ФДТ – индуцированного оксидантного стресса является гибель клеток, нарушение трофики и оксигенации ткани в результате ишемического повреждения сосудов опухоли. Эти процессы в свою очередь, запускают механизмы воспалительных иммунных реакций.

Рис.1. Зависимость реакции клеток на воздействие активных форм кислорода (АФК) от интенсивности процессов перекисного окисления липидов (ПОЛ).
Первичное тканевое повреждение, возникающее в опухоли после проведения ФДТ, служит пусковым моментом воспаления. Далее следует активация ряда эффекторных механизмов: вторичной воспалительной альтерации тканей, сосудистой реакции (вазодилатация, стаз, тромбоз, экссудация), реакция клеток крови (хемотаксис, фагоцитоз). Воспалительная реакция повреждает ткани, главным образом в результате нарушения системы кровоснабжения [44]. Как было показано рядом авторов, в опухолевой ткани сразу после окончания ФДТ можно наблюдать выраженное снижение кровотока. В сосудах микроциркуляции отмечается вазоконстрикция или вазодилатация, агрегация эритроцитов, стаз кровотока в опухолевых артериолах, тромбоз венул. Микрососудистый коллапс, наблюдаемый при ФДТ, лежит в основе опухолевой гипоксии/аноксии [26; 29; 40; 59; 6; 28]. Рядом исследований показано, что пусковым механизмом сосудистых эффектов ФДТ является: изменение метаболизма и последующий некроз эндотелиальных клеток, приводящий к их сепарации [19; 57]. Помимо эндотелия, деструктивные изменения затрагивают и другие компоненты сосудистой стенки, в частности, коллагеновые волокна экстрацеллюлярного матрикса [10]. Ведущую роль в повреждении клеток сосудов и изменении микроциркуляции при ФДТ играют медиаторы воспаления, продуцируемые, в основном, клетками миелоидного ряда (синглетный кислород, цитокины, простагландины и тромбоксаны) [30]. Эти вещества оказывают влияние на тонус сосудов, вызывают активацию факторов свертывания крови, агрегацию тромбоцитов [12; 19; 32; 38; 57].
Фотоокисление липидов и белков мембран клеток и сосудов опухоли является основным и наиболее существенным нарушением, которое индуцирует ФДТ в опухолях при использовании различных ФС [47]. Эти деструктивные изменения вызывают активацию фосфолипаз и ускоренную деградацию поврежденных мембранных фосфолипидов [18]. Массивное высвобождение фрагментов мембранных липидов и образование производных арахидоновой кислоты (тромбоксан, простагландины, лейкотриены) способствуют привлечению и активации клеток-эффекторов воспаления. Хемоаттрактантными свойствами обладают также формилпептиды, образующиеся в результате протеолиза белков в месте повреждения, компоненты комплемента, цитокины (IL-1, IL-6, IL-10, TNF –α, G-CSF) [24]. Аккумуляция клеток миелоидного ряда является ключевым событием развития воспалительной реакции в ткани опухоли после ФДТ. Последовательность этапов данного процесса представлена на рис. 2.
Первыми клетками иммунной системы, поступающими вместо локализации опухоли, являются нейтрофилы [50]. Накапливаясь в сосудах и периваскулярной области, нейтрофилы выделяют токсические продукты метаболизма кислорода и лизосомальные ферменты, индуцирующие повреждение сосудов опухоли и опухолевых клеток [37; 45; 61]. Нейтрофилы усиливают процесс иммунного воспаления и модулируют активность Т- и В- клеток посредством синтеза ряда цитокинов (IL-1, IL-6, TNF –α) [22; 52; 55]. Активизированные нейтрофилы быстро разрушаются с выделением хемотаксических факторов, привлекающих другие клетки, участвующие в процессе воспаления. Вслед за инвазией опухоли нейтрофилами в опухолевой ткани повышается количество тучных клеток [50]. Высвобождение содержимого гранул тучных клеток и хемоаттрактантов “погибших” нейтрофилов является сигналом для следующей волны инвазии воспалительными клетками, включая макрофаги и моноциты. В работе Bugelski P.J. et al. было показано, что макрофаги играют важную роль в дальнейшем развитии процесса в опухолевой ткани, обнаружившие, что клетками стромы, наиболее длительно задерживающими препарат, являются макрофаги, эти данные согласуются с результатами Krosl et al. [21; 49; 50]. Установлено, что опухоль – ассоциированные макрофаги способны накапливать в 9 раз больше порфиринов, чем клетки опухоли [36]. Избирательное накопления красителя макрофагами, как полагают, связано с их способностью захватывать липопротеины низкой плотности, которые являются переносчиками ФС в кровеносном русле. Повышение противоопухолевой активности макрофагов после ФДТ продемонстрировано в экспериментах как in vitro, так и in vivo [56; 61]. Эффект ингибирования опухолевого роста достигается в результате секреции токсичных для опухолевых клеток продуктов (АФК, лизосомальных ферментов, провоспалительных цитокинов), повышение фагоцитарной и киллерной активности макрофагов.

Рис. 2. Активация клеток миелоидного ряда и развитие воспалительной реакции после фотодинамического воздействия.
Так показано, что проведение ФДТ с мета- тетра- (гидроксиферил) хлорином вызывало повышение поглотительной способности макрофагов, синтеза TNF и продукции оксидов азота, цитотоксической активности клеток [27]. Облучение макрофагов в присутствии лимфоцитов приводило к увеличению их Fc-рецепторной активности [61]. Эффект зависел от дозы ФС и длительности облучения. Показано, что ФДТ с гематопорфиринами потенцировало цитотоксическую активность макрофагов in vitro в отношении опухолей А549 и SCCVII [47]. В то же время фотодинамическое воздействие вызывало лишь слабую стимуляцию активности макрофагов в культуре нормальных клеток почки. Предполагается, что макрофаги способны распознавать в опухолевых клетках потенциально репарируемые повреждения, индуцированные ФДТ, такие, например, как специфически измененные липидные фрагменты клеточных мембран, что помогает им идентифицировать их как клетки мишени. Повышение цитотоксической активности макрофагов при ФДТ, по- видимому, носит опосредованный характер. В пользу этого свидетельствуют данные о том, что фотодинамическое воздействие in vitro с использованием препарата гематопорфирина Фотоксан на высокоочищенную популяцию макрофагов не приводило к индукции цитотоксичности макрофагов в отношении опухолевых клеток YAC-1 [58]. вероятно, сигналом активации макрофагов при ФДТ является узнавание и фагоцитоз разрушенных опухолевых клеток. Развитие ФДТ – индуцированного воспаления сопровождается повышением синтеза фагоцитирующими макрофагами широкого спектра цитокинов: IL-1, IL-2, IL-10, IL-6, G-CSF, TNF-α, IFN-γ. [27; 31; 33; 35; 42]. Известно, что эти медиаторы контролируют критически важные этапы воспалительного процесса: индуцируют прокоагулянтную активность макрофагов и эндотелиоцитов, синтез адгезивных молекул, хемоаттрактацию лейкоцитов в очаг воспаления, стимулируют цитотоксичность гранулоцитов и макрофагов, усиливают фагоцитоз. Макрофагальные цитокины вовлекают в воспалительный процесс полиморфноядерные лейкоциты, эндотелиальные и другие клетки. Накопление нейтрофилов в ткани опухоли, повышение активности нейтрофилов и макрофагов, индуцированные ФДТ, существенны для получения положительных клинических результатов [27; 45]. Эти данные подтверждаются результатами исследований с использованием экспериментальных опухолевых моделей. Так, установлено, что удаление циркулирующих нейтрофилов у мышей с трансплантированными опухолями с помощью моноклональных ант-GR1 и инактивация макрофагов препаратами силикона уменьшает лечебный эффект ФДТ [45]. Таким образом, лечебные свойства ФДТ, помимо направленного цитотоксического эффекта, является результатом инициированной окислительным стрессом вторичной тумороцидной активности. Вторичные эффекты включают развитие воспалительной реакции, окклюзию сосудов опухоли и индукцию цитотоксической активности клеток воспаления в отношении опухолевых клеток.
Другим важным компонентом вторичного ответа являются опухолеспецифические иммунные реакции. Интенсивное разрушение клеток при ФДТ опухоли, опосредованное описанными выше механизмами, приводит к формированию противоопухолевого иммунитета. По мнению авторов работы Doughrti T.J., еt al., развитие специфической иммунной реакции включает несколько этапов. Первым этапом является активация опухоль – ассоциированных макрофагов и дендритных клеток, рекрутированных в область опухолевого узла медиаторами воспаления (рис.3) [29].
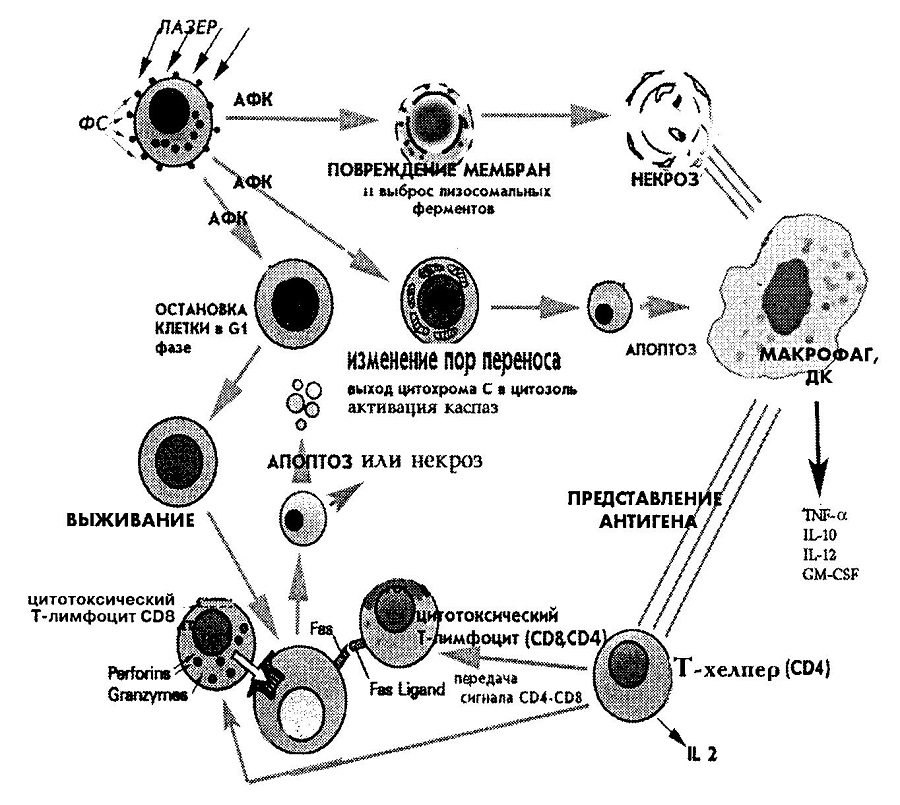
Рис. 3. Стадии развития специфического иммунного ответа после проведения ФДТ.
Эти клетки принимают участие в представлении иммунокомпетентным клеткам антигенов убитых или поврежденных ФДТ опухолевых клеток, а также продуктов воспалительной деструкции опухолевой ткани. Антигенпредставляющие клетки (АПК) осуществляют процессинг опухолевых антигенов и презентируют их на своих мембранах в комплексе с антигенами ГКГС. представление опухолевых антигенов сопровождается стимуляцией Т – хелперов, которые, в свою очередь, индуцируют процесс формирования популяции опухоль специфических цитотоксических Т – клеток. Активированные цитотоксические Т- лимфоциты взаимодействуют с опухолевой клеткой, вызывая ее гибель посредством двух основных механизмов. При контакте CD8+ Т- лимфоцитов перфорин – и гранзимсодержащие гранулы этих клеток высвобождают свое содержимое в щель между цитотоксической клеткой и ее мишенью, вызывая разрушение клетки – мишени.
Второй механизм цитотоксического действия заключается в передаче сигнала апоптоза через FAS – лиганд, содержащийся на поверхности активированных CD4+ и CD8+ Т- лимфоцитов. Важной особенностью ФДТ – индуцированного иммунного ответа является доминирование клеточного звена. Показано, что лизаты опухолевых клеток, обработанных ФДТ, обладают высокой иммуногеннстью и активируют преимущественно Т-клеточный иммунитет [34]. Популяции сенсибилизированных лимфоцитов имеют существенное значение для предотвращения роста опухоли, подвергнутой ФДТ. Показано, что селективная элиминация цитологических Т – клеток макрофагов и нейтрофилов непосредственно после ФДТ приводила к существенному снижению противоопухолевого эффекта терапии [45]. Аналогичные результаты наблюдались после селективной элиминации Т – хелперов. Установлено, что CD8+ Т – клетки необходимы для предотвращения рецидива опухоли после проведения ФДТ. Проведение ФДТ с применением бензофенотиазина ингибировало рост фибросаркомы ЕМТ-6 у 75% мышей, но не влияло на рост опухоли у Т – дефицитных мышей. Селективное удаление Т – клеток с использованием CD8+ антител снижало эффективность терапии [41]. ФДТ – индуцированный иммунитет вносит значительный вклад в отдаленные противоопухолевые эффекты фотодинамического воздействия. В работе Korbelik M. et al., было показано что, адоптивный перенос сенсибилизированных к ЕМТ6 опухолевым клеткам спленоцитов BALB/с мышей, излеченных после ФДТ, вызывали ингибирование роста опухоли при проведении ФДТ с использованием фотофрина. Лечебный эффект наблюдался как у мышей с острым комбинированным иммунодефицитом (severe combined immunodeficient, SCID), так и у иммунокомпетентных мышей линии BALB/с. Восстановление иммунодефицита у SCID мышей с ЕМТ6 опухолью спленоцитами от иммунологически интактных BALB/с мышей не улучшало эффекта ФДТ. Селективное удаление популяции специфических Т – клеток из трансплантируемых спленоцитов показало, что основными клетками эффекторами, ответственными за лечебный эффект ФДТ, являются цитологические лимфоциты, в то время как Т – хелперы играют роль посредников [46].
ФДТ индуцированная активность сенсибилизированных к опухолевым антигенам лимфоцитов не ограничивается областью воздействия, затрагивая метастазирующие опухолевые клетки. Так, у мышей с полной регрессией опухоли ЕМТ6 после ФДТ наблюдали ингибирование роста опухоли после повторной прививки опухолевых клеток [41]. Проведение ФДТ в комплексе с иммунотерапией вызывало формирование противоопухолевой резистентности к вторичной прививке опухолевых клеток, увеличению времени жизни животных и уменьшение количества метастазов [25].
Ряд данных свидетельствует о важной роли, которую играют в процессе ингибирования опухолевого роста натуральные киллеры (NK). Показана активация NK – клеток после проведения ФДТ у экспериментальных животных с Meth-A саркомой [46]. Удаление натуральных киллеров (NK) in vivo с помощью anti-asialo-GM1 антител значительно уменьшало эффект ФДТ с применением бензофенотиазина. Однако NK селезенки, донорами которых были мыши-опухоленосители после ФДТ, не оказывали цитотоксического эффекта в отношении ЕМТ6 опухолевых клеток in vitro, что свидетельствует об опосредованном характере эффекта [41].
Схематическое изображение механизмов противоопухолевых эффектов ФДТ представлено на рис.4. Вклад того или иного звена в формирование противоопухолевого иммунитета, как можно предполагать, зависит от типа используемого ФС и специфических особенностей опухоли.
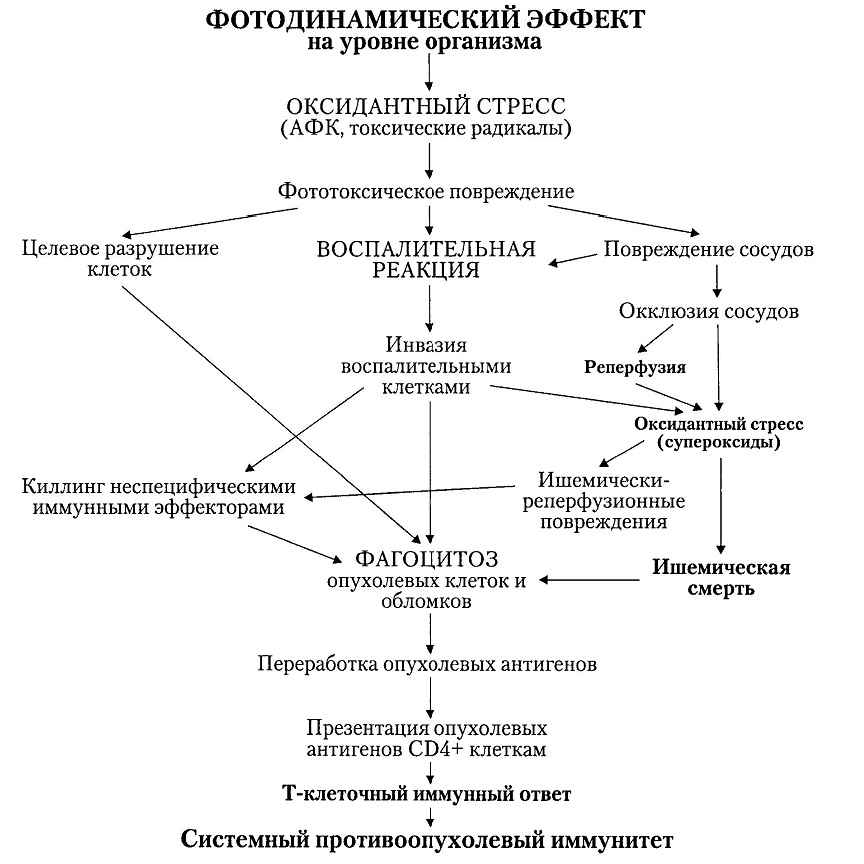
Рис. 4 Основные механизмы противоопухолевого эффекта ФДТ.
В Центре Избирательной Хронотерапии и ГУ НИИЭМ им. Н.Ф. Гамалеи РАМН был проведен ряд исследований по определению иммунного статуса у больных после стандартного противоопухолевого лечения (химиотерапия, лучевая терапия, хирургическое вмешательство) на фоне применения метода избирательной хронофототерапии. В результате фотодинамического воздействия наблюдались существенные изменения в иммунной системе больных, что и учитывалось в реабилитационном периоде.
В первое исследование было включено 50 больных раком молочной железы (РМЖ) и 49 больных опухолями головного мозга (ОГМ) до и на фоне применения ИХФТ. Наблюдение проводили в течение 4-6 месяцев от начала курса иммунокоррекции. Эффективность ИХФТ оценивали по следующим показателям: количественное содержание лейкоцитов, лимфоцитов и нейтрофилов периферической крови; субпопуляционный состав лимфоцитов (CD3, CD4, CD8, CD16/56, CD19, CD38, CD54, CD71, CD95); соотношение иммунорегуляторных Т-лимфоцитов (CD4/CD8). Обработку полученных результатов проводили общепринятыми статистическими методами с помощью программы FoxPro. У 40% больных РМЖ обнаруживался нейтрофильный лейкоцитоз и подавление лимфоцитарного ростка. У больных с ОГМ в 50% случаев отмечалась лейкопения как лимфоцитарного (31%), так и нейтрофильного (27%) характера. У больных обеих групп выявлен дисбаланс между Т, В – и NK-клетками. Установлено, что при ОГМ недостаточность Т-клеток связана как с подавлением хелперного звена (CD4), так и цитотоксических лимфоцитов (CD8) (CD4/CD8 = 1.0-1.1). У 80% больных РМЖ отмечалась выраженная недостаточность CD8-лимфоцитов, причем 25% имели гиперэкспрессию CD4 (СD4/СD8=2.6-3.1). И в той, и в другой группе больных возрастало количество В-лимфоцитов и NK-клеток, в 2-2.5 раза превышающее физиологическую норму. Исследование маркеров активации и апоптоза иммунных клеток выявило выражено сниженную способность лимфоцитов к апоптозу (CD95) и высокую экспрессию CD71 (активированные В-клетки). У больных РМЖ в большей степени, чем у лиц с ОГМ наблюдалось нарушение дифференцировки лимфоцитов, проявляющееся в снижении экспрессии CD38. При ОГМ в значительной степени отмечались нарушения в моноцитарно-макрофагальной системе, о чем судили по низкому уровню экспрессии CD54. Через 1 месяц после начала реабилитационного курса методом ИХФТ у 96% больных РМЖ и 91% ОГМ отмечалась положительная динамика, пришло в норму содержание нейтрофилов и лимфоцитов. Как при РМЖ, так и при ОГМ экспрессия CD95 повышалась до физиологической нормы у 95% и у 87% больных соответственно. Более чем у половины больных как РМЖ, так и ОГМ высокая экспрессия CD71 достигала физиологически нормального уровня. У остальных отмечалась выраженная тенденция к ее снижению. Было отмечено не только корректирующее, но и иммуномодулирующее действие ИХФТ. Так, у больных ОГМ с недостаточностью CD8-лимфоцитов и повышенным уровнем CD4-клеток отмечалось достоверное количественное увеличение CD8 и снижение до уровня нормы CD4-лимфоцитов. В то же время, у больных, имевших недостаточность либо Т-хелперов (CD4), либо цитотоксических Т-лимфоцитов (CD8) наблюдалось повышение уровня только дефицитных клеток, при этом физиологически нормальное количество клеток сохранялось. У больных РМЖ достоверно повышалась экспрессия CD38, что свидетельствовало о восстановлении механизмов дифференцировки лимфоцитов. У лиц с ОГМ увеличение экспрессии CD54 указывало на восстановление функций моноцитарно-макрофагальной системы. При последующих иммунологических исследованиях в течение 4-6 месяцев отмечалась стабилизация восстановленных иммунологических показателей[1].
Во второе исследование было включено 18 больных со злокачественными опухолями головы и шеи III-IV стадии. Проведено иммунологическое исследование, направленное на выявление нарушений в клеточном иммунитете. Методом иммунофенотипирования определяли следующие маркеры лимфоцитов: CD3, CD4, CD8, CD16, CD19, CD38, CD54, CD71, CD95.
У всех больных отмечались: недостаточность Т – клеточного звена иммунитета, нарушения в системе моноцитов/макрофагов, низкая способность лимфоцитов к апоптозу, завышенный уровень NK-клеток и неактивированных В-лимфоцитов. В ходе терапии методом ИХФТ с хлорином Е6 количество Т-лимфоцитов резко увеличивалось за счет возрастания Т-хелперов (50%) и/или цитотоксических Т-лимфоцитов (50%). Возрастал уровень активации Т и В-клеток (CD38), моноцитов/макрофагов (CD54). Отмечалась тенденция к повышению экспрессии CD95 – маркера апоптоза. Одним из критериев оценки тяжести опухолевого процесса является высокий уровень экспрессии CD71. У первичных больных этот показатель на 7-10% превышал физиологическую норму. После проведения ИХФТ экспрессия CD71 снижалась в 2 раза [2].
В следующем исследовании процедуры ИХФТ были проведены 72 больным с глиомами мозга и опухолями шеи. Цель работы – разработка методики деструкции глубокорасположенных опухолей и комплекса реабилитации онкологических больных после хирургического, лучевого и химиотерапевтического лечения. Использованы лазерные диодные модули ML500-SP и Sunny (PDT-662), предназначенные для ФДТ с хлорином Е6 и цифровой индикацией интенсивности флюоресценции. С помощью дополнительного устройства биоуправления по сигналам с датчиков пульса и дыхания, установленных на теле пациента, осуществлялась биосинхронизация лазерного воздействия только в фазах выдоха и диастолы (моменты уменьшения кровенаполнения ткани). Плотность мощности, длительность воздействия и соотношения глубин амплитудной модуляции несущей частоты 22,5 кГц по сигналам пульса, дыхания и тремора были выбраны и в соответствии размерами и типом опухоли, с наличием и характером дисбаланса артериальной и венозной частей капиллярного русла в месте локализации опухоли. У 14% больных был отмечен полный эффект, что указывало на перспективность использованной методики. Фактическое отсутствие интоксикации у больных, подвергавшихся ФДТ в режиме биоуправления, свидетельствовало в пользу предположения об индукции апоптоза клеток опухоли со стороны поверхностно расположенных клеток. Лазерная биосинхронизация ритмов золь-гель переходов в этих клетках, вероятно, обеспечивает генерацию собственных излучений этих нормальных клеток, воздействующих на клетки опухоли [3].
В другом исследовании было обследовано 21 больной с злокачественными новообразованиями различной локализации, проходивших сеансы ИХФТ с апреля по ноябрь 2007 года. Уровень опухоль – ассоциированных антигенов определяли методом ИФА. Иммунологическое исследование включало: определение субпопуляций лимфоцитов (CD3, CD4, CD8, CD16, CD19, CD56) методом иммунофенотипирования; оценку нейтрофильного фагоцитоза в латекс – и НСТ – тестач; определение концентраций сывороточных lgA, lgG, lgM по Mancini G. et. al; спектрофотометрический анализ ЦИК, подсчет лейкоцитов, лимфоцитов, нейтрофилов, моноцитов и эозинофилов в венозной крови. При сравнении исследуемых показателей до и после проведения ИХФТ были выявлены статистически достоверные изменения лейкоцитов в 1 л крови. Так, у больных с лейкопенией (3.5±1.2 109/л) после 6-10 сеансов ИХФТ количество лейкоцитов увеличивалось до уровня физиологической нормы (7.0±2.5 109/л) и у двоих – превышало его. У 6 больных с изначально нормальным количеством лейкоцитов отмечался лейкоцитоз (9.5±2.1 109/л). Данное дисгармоничное явление может быть связано с ускорением разрушения опухолевых клеток и возникающей вследствие этого интоксикацией организма, клинически проявляющейся повышением температуры тела до субфебрильной. Во всех случаях лейкоцитоз проявлялся увеличением относительного содержания нейтрофилов до 72.0±5.0 109/л, что, вероятно, связано с формированием некротического очага. Кроме этого, в результате исследования была обнаружена положительная динамика Т-хелперов, количество которых возрастало с 28.0±5.0% до 34.0±6.0%, что, в свою очередь, приводило к гармоничному соотношению между Т-хелперами и Т-супрессорами. Индекс иммунорегуляции на фоне ИХФТ повышался с 1.0±1.2 до 1.5±1.3.
Статистически достоверные результаты получены при анализе B-лимфоцитов и NK-клеток. Так, у большинства обследованных больных количество B-клеток в 2 раза превышало физиологическую норму и составляло 21.0±5.0%. После 6-10 сеансов ИХФТ более чем у половины больных количество B-лимфоцитов снижалось до уровня физиологической нормы, а количество NK-клеток увеличивалось с 11.0±4.0% до 16.0±5.0%. Увеличение доли естественных киллеров, вероятно, связано с мобилизацией неспецифических механизмов противоопухолевой защиты.
У обследованных нами больных низкая способность к завершенному фагоцитозу обнаруживалась у 5 человек. В то же время у трети больных, по данным спонтанного НСТ-теста, выявлена повышенная активация кислородозависимого метаболизма, свидетельствующая об усилении хемотаксиса и бактерицидности фагоцитов, что в состоянии незавершенного фагоцитоза, часто встречающегося при онкогенезе, что может привести к ускорению роста опухоли. После проведения сеансов ИХФТ у 90% больных с такого рода нарушениями происходило снижение спонтанной активации нейтрофилов до нормальных значений при одновременном возрастании их фагоцитирующей функции. При исследовании гуморального звена иммунитета у обследуемых больных выявлено повышение концентрации lgM (4 человека), снижение уровня lgG (8 человек) и у 3 больных был повышен уровень lgA. В результате проведенной ИХФТ концентрация иммуноглобулинов практически достигала уровня физиологической нормы: у 4 больных синтез lgM, вероятно, переключался на синтез lgG, о чем свидетельствовали высокие концентрации последнего в сыворотке крови. При исследовании ЦИК в сыворотке крови был отмечен их повышенный уровень у половины обследуемых больных, который значительно снижался после 3-4 сеансов ИХФТ. Установленный факт является значимым показателем эффективности проведенной терапии, поскольку ЦИК, блокируя антигенраспознающие Т-лимфоциты, снижают их противоопухолевую активность. При совокупном анализе показателей иммунного статуса и концентраций опухоль-ассоциированных маркеров было замечено, что у больных с гармоничным соотношением иммунорегуляторных Т-лимфоцитов (ИРИ=1.3-1.7), достигнутым с помощью ИХФТ, концентрации опухоль-ассоциированных антигенов значительно снижалась. При этом увеличение доли Т-лимфоцитов на фоне снижения количества B-клеток и нормализация уровня иммуноглобулинов в сыворотке так же сопровождалось снижением уровня опухоль – ассоциированных маркеров [4].
В следующем исследование было включено 200 больных различными злокачественными заболеваниями. Нарушения клеточного и гуморального иммунитета имели место практически у всех исследованных больных.
При ИХФТ воздействие в фазах диастолы и выдоха снижало эффективную плотность мощности благодаря уменьшению теплоемкости ткани в моменты снижения кровенаполнения. Снижение необходимой для ФДТ эффекта плотности мощности в периоды уменьшения кровенаполнения опухолевой ткани происходило за счет уменьшения затрат энергии на нагрев крови. При этом уменьшалась и теплопроводность ткани. В результате уменьшалась зона тепловой денатурации и некроза окружающей здоровой ткани.
Метод биосинхронизации и биохронотерапии основан на экспериментальном изучении взаимосвязи ритмов биосинтеза, функции и энергетики на уровне отдельной клетки. Полученные результаты привели к выводу о воздействии лазерного излучения на опухоли глубокой локализации. Возможность воздействия на опухоли глубокой локализации связана с особенностью проникновения лазерного света в биологическую ткань.
Вопрос о глубине проникновения излучения в ткань не вполне ясен. Наблюдаемым фактом является то, что лазерное излучение с длиной волны λ -662 нм стимулирует свечение из мест накопления хлорина с глубины порядка 1 см. Исходя из этого, необходимо предположить, что характерная длина поглощения этого излучения в биоткани более 1 см. При этом с точки зрения физики биоткань, является сильно рассеивающей средой. Характерная длина рассеяния излучения в биоткани меньше характерной длины поглощения. Поэтому распространение излучения в биоткани носит диффузионный характер. Известно, что при меньших длинах волн существенно поглощение за счет возбуждения электронных степеней свободы различных красящих веществ, при больших длинах волн существенно поглощение на колебательно-вращательных переходах воды. Столь большая длина поглощения связана с наличием окна прозрачности в области ~ 600÷700 нм. В этом окне прозрачности расположена полоса поглощения хлорина Е6. Лазерное излучение приводит к возбуждению электронных степеней свободы хлорина-Е6. Некоторая часть продуктов возбуждения излучает в диапазоне более 662 нм и некоторая доля этого излучения проникает наружу.
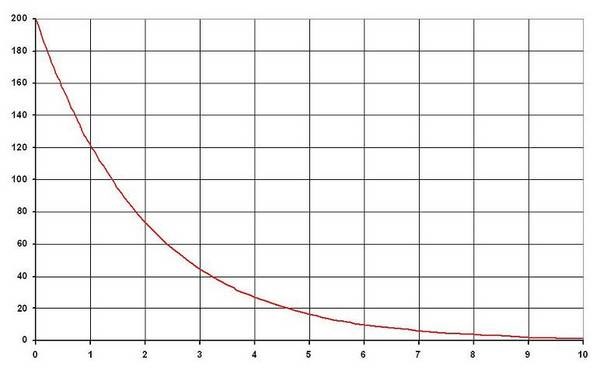
Рис. 5. Проникновение лазерного света с длиной волны 662 нм в биологическую ткань.
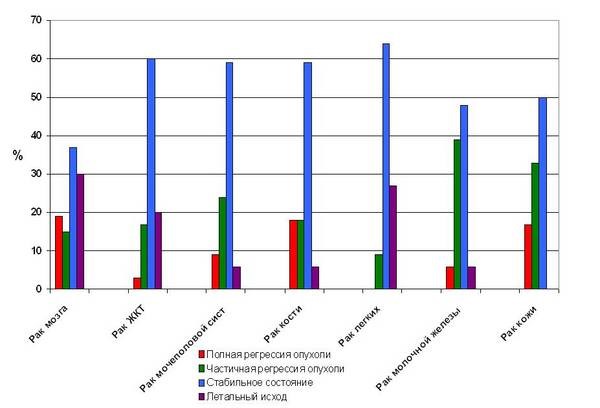
Рис. 6. Статистические данные анализа реабилитационного лечения методом ИХФТ.
Учитывая выше сказанное, на рисунке 5 представлено вероятное усредненное изменение эффективной мощности лазерного света с длиной волны 662 нм (применяется с современными сенсибилизаторами в ФДТ) при взаимодействии с биологической тканью. На рисунке 5 приведен усредненный эффект, т.к. не учитывается влияние различных видов биотканей. В режиме автоматической синхронизации лазерного воздействия с ритмами центрального кровотока обнаружена нормализация уровня и спектра ритмов микроциркуляции крови в месте патологии. В режиме синхронизации импульсов оказалось возможным по комплексу показателей реакций на клеточном, тканевом и организменном уровнях определить оптимальные параметры лазерного излучения. На основании полученных результатов были разработаны и изготовлены аппараты для ИХФТ.
На рисунке 6 представлены данные статистического анализа реабилитационного лечения методом ИХФТ. В клинических испытаниях при различных заболеваниях доказана эффективность метода ИХФТ. Эффективность обусловлена, отсутствием негативных побочных реакций, расширением терапевтического диапазона параметров интенсивности, стабильностью лечебного эффекта, при образовании тканевой памяти, использованием биологического таймера вместо физического,
ускорением восстановительного процесса, за счет учета характера местной патологии, с применением адекватного соотношения глубин амплитудной модуляции по пульсу, дыханию, тремору, в отсутствии адаптации к уровню физиотерапевтического воздействия, за счет неравномерности дыхания и пульса больного [5].
В другом исследование изучены результаты лечения и реабилитации 90 больных, из них 13 РМЖ. В качестве контроля служили больные, которым применялась ФДТ с лазерным воздействием тех же параметров без биоуправления. Для достижения лечебного эффекта и успешной реабилитации пациентам данной группы повторно вынуждены были проводить ФДТ в режиме биоуправления. У 10 больных раком молочной железы предшествовала химиотерапия, у четырех из них ДЛТ. У 8 человек имелись метастазы в регионарные лимфоузлы, у 5 –метастазы в печень и кости позвоночника, метастазы в отдаленные лимфатические узлы – у 6 больных РМЖ. Снижение и различные нарушения клеточного и гуморального иммунитета имели место практически у всех исследованных больных. Поскольку сама ФДТ могла снижать клеточный иммунитет, для закрепления положительного результата проводили повторные курсы повышения клеточного иммунитета с помощью биоуправляемой магнитолазерной терапии. Метод биосинхронизации и биохронотерапии основан на экспериментальном изучении взаимосвязи ритмов биосинтеза, функции и энергетики на уровне отдельной клетки. С помощью прижизненной интерференционной микроскопии и регистрации ритмов содержания белка, электрофизиологической регистрации ритмов функциональной активности, микрокиноденситографии ритмов агрегации митохондрий и микрополярографического измерения ритмов напряжения кислорода была доказана энергетическая параметрическая зависимость функциональной индукции пластических процессов. Эта закономерность была подтверждена на тканевом, органном и организменном уровне. Для разных видов физиотерапии было установлено, что физические воздействия на ткань или орган в фазах увеличения кровенаполнения и увеличения энергообеспечения ответных реакций, усиливают преимущественно биосинтетические восстановительные процессы, а в фазах снижения энергетики преимущественно деструктивные процессы. В режиме автоматической синхронизации лазерного воздействия с ритмами центрального кровотока обнаружена нормализация уровня и спектра ритмов микроциркуляции крови в месте патологии. Режим биоуправления исключает неопределенность и непредсказуемость направленности интегральных реакций ткани, органа и организма на физиотерапевтическое воздействие за счет автоматического учета исходного состояния биосистемы. В режиме биоуправления оказалось возможным по комплексу показателей реакций на клеточном, тканевом и органном уровнях определить оптимальные параметры лазерной терапии и ФДТ. При этом были использованы показатели реакции разжижения или желатинизации цитоплазмы (ритмы золь-гель переходов), уровень и спектр ритмов микроциркуляции крови, активность супероксиддисмутазы эритроцитов крови, вегетативный статус, клеточный иммунитет и некоторые другие диагностические показатели. На основании полученных результатов были разработаны и изготовлены аппараты для биоуправляемой лазерной терапии, ФДТ и другим видам биохронотерапии.
Возможность воздействия на опухоли глубокой локализации связана с особенностью проникновения лазерного света с рабочей длиной волны в биологическую ткань и с условиями биосинхронизации с ритмами золь-гель переходов в клетках поверхностных слоев, воспринимающих непосредственно лазерное воздействие. Первое предположение, объясняющее фактически наблюдаемый эффект, состоит в том, что этот эффект обусловлен не только не посредственно проникшими в ткань фотонами, но и индукцией цепной реакции образования активных форм кислорода в зоне локализации ФС. Другое предположение основано на отличии эффекта при обычной ФДТ и ФДТ в режиме биоуправления, что можно объяснить переизлучением, возникающим уже в наружных нормальных клетках благодаря синхронизации ритмов лазерного воздействия с ритмами золь-гель переходов в этих клетках, синхронных в свою очередь с ритмами микроциркуляции крови и открытием капилляров в чередующихся ансамблях клеток с большей чувствительностью. Такая эстафетная ретрансляция сигналов может компенсировать поглощение на пути к локализации ФС в относительно глубокорасположенной опухоли. В пользу этого предположения свидетельствует более сильное свечение опухоли при одних и тех же параметрах лазерного излучения в случае режима биосинхронизации. Это явление и используется при реабилитации больных с глубокими локализациями опухолей. Обнадеживающие результаты получены при терапии у прооперированных пациентов, в том числе и при дальнейшем метастазировании.
Список литературы.
- Борисов В.А., Гусева О.А. Иммунокорректирующее действие избирательной хронофототерапии при раке молочной железы и опухолях головного мозга. Центр Биохронотерапии, Москва, Биомед им. И.И. Мечникова.
- Борисов В.А., Гусева О.А., Григорян С.С. Применение избирательной хронофототерапии с хлорином Е6 у больных с злокачественными новообразованиями в области головы и шеи: особенности клеточного иммунитета. Журнал Онкохирургия том 1, №2, 2009 г.
3. Борисов В.А., Загускин С.Л. Биоуправляемая фотодинамическая терапия и реабилитация онкологических пациентов. Журнал Онкохирургия том1,№2,2009г.
4. Борисов В.А., Гусева О.А., Григорян С.С. Изменение показателей иммунного статуса у пациентов с онкологическими заболеваниями после проведения избирательной хронофототерапии. Национальная конференция «Аллергология и клиническая иммунология – междисциплинарные проблемы», Москва, февраль 2008г.
5. Борисов В.А. Реабилитация онкологических больных методом избирательной хронофототерапии. Берлин, апрель 2007 г. - Борисов В.А. Особенности реабилитации онкологических больных сочетанием фотодинамической терапии и биохронотерапии. Доклад на Втором Междисциплинарном конгрессе по проблеме рака молочной железы. Берлин, май 2006г.
7. Борисов В.А., Гусева О.А. Избирательная Хронофототерапия как перспективный метод для ускоренного восстановления иммунологических нарушений у тяжелых онкологических больных и улучшения их клинического состояния. ФГБУ “ФНКЦ детской гематологии, онкологиии иммунологии им. Дмитрия Рогачева”, Москва 2007 г.
8. Борисов В.А. Особенности реабилитации онкологических больных сочетанием фотодинамической терапии и биохронотерапии. Доклад. Междисциплинарный конгресс по проблемам рака молочной железы, Берлин, май, 2006 г. - Васильев Н.Е., Сысоева Г.М., Даниленко Е.Д. Иммунологические аспекты фотодинамической терапии. Медицинская Иммунология 200, Т.5, №5-6, стр. 507-518.
- Гельфонд М.Л. Фотодинамическая терапия в онкологии. Практическая онкология 2007, Т. 8, № 4.
- Давыдов М.И. Снеговой А.В. Поддерживающая терапия в онкологии. Газета Российского общества клинической онкологии. Выпуск 10-11 • 2015 г.
- Кац В.А., Литвин Г.Д., Назаров Ш.П., Ряжский Г.Г., Странадко Е.Ф., Якубов А.С., Градюшко А.Т., Иванов А.В. Фотодинамическая терапия. Вопросы онкологии, 1992 г.,Т.38, №12, стр. 1403-1412.
- Коган Е.А., Невольских А.А., Жаркова Н.Н., Лощенов В.Б. Морфо- и патогенез повреждений злокачественных опухолей при фотодинамической терапии. Архив патологии, 1993 г., №6, стр.73-76.
- Кудинова Н.В., Березов. Т.Т. Фотодинамическая терапия опухолей: иммунологический аспект лечения. Российский биотерапевтический журнал 2010 г., Т. 9, № 1.
- Кузнецова Н.А., Калия О.Л. Фотокаталитическая генерация активных форм кислорода в биологических средах в методе фотодинамической терапии. Российский химический журнал, 1998 г., Т.42, №5, стр.155-171.
- Моисеенко В.М. Практические рекомендации по лекарственному лечению злокачественных опухолей (RUSSCO). Российское общество клинической онкологии 2015 г.
- Меньшикова Е.Б., Зенков Н.К. Окислительный стресс при воспалении. Усп. соврм. биол., Т.117, вып. 2, стр.155-171.
- Agarwal M.L., Larkin H.E., Zaidi S.I., Mukhtar H., Oleinick N.L. Phospholipase activation triggers apoptosis in photosensitized mouse lymphoma. Cancer Res., 1993, Vol.S3, № 24, P.SS97-S902.
- Berenbaum M.C., Hall G.W., Hoyes A.D. Cerebral photosensitization by hematoporphyrin derivatie. Evidence for an endothelial site of action. Brit. J. Cancer,1986, Vol.53, №1, Р.81-89.
- Bernardi P., Scorano L., at all. Mitochondria and cell death. Mechanistic aspects and methodological issues. Eur. J. Biochem., 1999, Vol.264, №3, Р.687-701.
- Bugelski P.J., Porter C.W., Dougherty T.J. Autoradiographic distribution of hematoporphyrin derivatie in normal and tumor tissue of the mouse. Cancer Res., 1981, Vol.183, №1, Р.43-51.
- Cassatella M.A. Neutrophil-derived proteins: sellingcytokines by the pound. Adv. Immunol., 1999,Vol.73, P.369-509.
- Cole W.H., Humphrey L. Need for immunologic stimulators during immunosuppression produced by major cancer surgery. Ann. Surg., 1985, Vol. 202, P. 9–20.
- Cecic I., Korbelik M. Mediators of peripheral blood neutrophilia induced by photodynamic therapy of solid tumors. Cancer Lett., 2002, Vol.153, P.43-51.
- Chen W.R., Adams R.L., Carubelli R., Nordquist R.E. Laser-photosensitizer assisted immunotherapy: a novel modality for cancer treatment. Cancer Lett., 1997, Vol.115, P.25-30.
- Chen G., Chen H., Hetzel F.W. Tumor oxygenation changes post-photodynamic therapy. Photochem. Photobiol., 1996, Vol.63, №1, Р.128-131.
- Coutier S., Bezdetnaya L., Marchal S., Melnikova V., Belitchenko I., Merlin J.L., Guillemin F. Foscan (mTHPC) photosensitized macrophage activation: enhancement of phagocytosis, nitric oxide release and tumor necrosis factor-alpha-mediated cytolitic activity. J .Cancer, 1999, Vol.51, №1. – P.37-42.
- de Vree W.J., Essers M.C., at all. Role of interleukin 1 and granulocyte-colony-stimulating factor in photofrin-based photodynamic therapy of rat rhabdjmyosarcoma tumors. Cancer. Res, 1997, Vol. 57, №13, Р.2555-2558.
- Doughrti T.J., Gomer C.J., Henderson B.W., Jori G., Kеtssel D., Korbelic M. еt all. Photodynamic therapy J. Natl/ Cancer Inst., 1998, Vol.90, №12, Р.889-905.
- Doughrti T.J., Tracker J.D., at all. Effect of immunization with genetically-modified tumor cells on tumor recurrence following photodynamic therapy. Lasers Med. Sci., 1992, Vol.7, Р.226-234.
- Evans S., Matthews W., Perry R., Fraker D., Norton J., Pass H.I. Effect of photodynamic therapy on tumor necrosis factor production by murine macrophages. J. Natl. Cancer Inst., 1990, Vol.82, № 1. – P.34-39.
- Fingar V.H., Wieman T.J., Doak K.W. Role of thromboxane and prostacyclin release on photodynamic therapy-induced tumor destruction. Cancer Res., 1990, Vol.50, №9, Р.2599-2603.
- Gollnick S.O., Liu X., Owczarczak B., Musser D.A., Henderson B.W. Altered expression of interleukin 6 and interleukin 10 as a result of photodynamic therapy in vivo. Cancer Res., 1997, Vol.57, № 18, P.3904-3909.
- Gollnick S.O., Vaughan L., Henderson B.W. Generation of effective antitumor vaccines using photodynamic therapy. Cancer Res., 2002, Vol.62, № 6, P.1604-1605.
- Gomer C.J., Luna M., Ferrario A., Wong S., Fisher A.M., Rucker N. Cellular targets and molecular responses associated with photodynamic therapy. J. Clin. Laser Med. Surg., 1996, Vol.14, №5, P.315-321.
- Hamblin M.R., Newman E.L. On the mechanism of the tumourlocalising effect in photodynamic therapy. J. Photochem. Photobiol. B., 1994, Vol.23, № 1, P.3-8.
- Hernandez L.A., Grisham M.B., Twohig B., Arfors K.E., Harlan J.M., Granger D.N. Role of neutrophils in ischemia-reperfusion-induced microvascular injury. Am. J. Physiol., 1987, Vol.253, №3, Р. 699-703.
- Henderson B.W., Dougherti T.J. How does photodynamic therapy work? Photochem. Photobiol., 1992, Vol.55, №1, Р.145-157.
- Henderson B.W., Stnik-Busch T.M., Vaugha L.A. Potentiation of photodynamic therapy antitumor activity mice by nitric oxide synthase inhibition is fluence rate dependent. Photochem. Photobiol.,1999, Vol. 69, №1, Р.64-71.
- Henderson B.W., Vaugha L.A. at all. Photosensitization of murine tumor, vasculature and skin by 5-aminolevulinic acid-induced porphyrin. Photochem. Photobiol.,1995, Vol.62, №4, Р.780-789.
- Hendrzak-Henionj.A., Knisely T.L., Cincotta L. Cincotta E., Cincotta A.H. Role of the immune system in mediating the antitumor effect of benzophenothiazine photodynamic therapy. Photochem. Photobiol., 1999, Vol.69, №5, P.575-581.
- Herman S., Kalechman Y., Gafter U., Sredni B., Malik Z. Photofrin II induces cytokine secretion by mouse spleen cells and human peripheral mononuclear cells. Immunopharmacology. 1996, Vol.31, №2-3, P.195-204.
- Jori G. Photosensitized processes in vitro: proposed phototherapeutic applications. Photochem. Photobiol., 1990, Vol.52, №2, P.41-43.
- Korbelik M. Induction of tumor immunity by photodynamic therapy. J. Clin. Laser Med. Surg., 1996, Vol.137, №1, Р.91-98.
- Korbelik M, Cecic I. Contribution of myeloid and lymphoid host cells to the curative outcome of mouse sarcoma treatment by photodynamic therapy. Cancer. Lett., 1999, Vol.137, №1, P.91-98.
- Korbelik M., Dougherty G.J. Photodynamic therapy-mediated immune response against subcutaneous mouse tumors. Cancer Res., 1998, Vol.59, №8, P.1941-1946.
- Korbelik M., Krosl G. Enhanced macrophage cytotoxicity against tumor cells treated with photodynamic therapy. Photochem. Photobiol., 1994, Vol.60, P.497-S02.
- Korbelic M., Parcins C., et all. Nitric oxide production by tumor tissue: impact on the response to photodynamic therapy. Br. J. Cacer.-2000.-Vol.82, №11.- Р.1835-1843.
- Krosl G., Korbelik M. Potentiation of photodynamic therapy by immunotherapy: the effect of schizophyllan (SPG). Cancer Lett., 1994,Vol.84, № 1, P.43-49.
- Krosl G., Korbelik M., Dougherty G.J. Induction of immune cell infiltration into murine SCCVII tumor by photofrin-based photodynamic therapy. Br. J. Cancer., 1995, Vol.71, №3, P.549-555.
- Lam M., Oleinick N., Nieminen A. Photodynamic therapy-induced apoptosis in epidermoid carcinoma cells. Reactive oxygen species аnd mitochondrial inner membrane permeabilization. J. Biol. Chem., 2001, Vol. 276, №50, Р.47379-47386.
- Lloyd A.R., Oppenheim J.J. Poly’s lament: the neglected role of the polymorphonuclear neutrophil in the afferent limb of the immune response. Immunol. Today., 1992, Vol.13, №5, P.169-172.
- Minamikawa T., Sriratana A., Chloromethyl-X-rosamine (Mito Tract Red) photosensitis mitochondria and apoptosis in intact human cells. J. Cell Sci., 1999, Vol. 112, №14, Р.2419-2430.
- Ng C.S. Thoracotomy is associated with significantly more profound suppression in lymphocytes and natural killer cells than video-assisted thoracic surgery following major lung resections for cancer. J. Invest. Surg., 2005, Vol. 18, P. 81–85.
- Oehler L.O., Majdic W.F., Pickl J., Stocki J., Riedl E., Drach J., Rappersberger K., Geissler K., Knapp W. Neutrophil granulocyte-committed cells can be driven to acquire dendritic cell characteristics. J. Exp. Med., 1998, Vol.187, P.1019-1028.
- Qin B., Selman S.H., Payne KM., Keck R.W., Metzger D.W. Enhanced skin allograft survival after photodynamic therapy. Association with lymphocyte inactivation and macrophage stimulation. Transplantation, 1993, Vol.56, №6, P.1481-1486.
- Reed M.W., Wieman T.J., at all. A comparison of the effect of photodynamic therapy on normal and tumor blood vessel in the rat microcirculation. Radiat. Res., 1989, Vol. 119, №3, Р.542-552.
- Reiter I., Schwamberger G., Krammer B. Activation of macrophage tumoricidal activity by photodynamic treatment in vitro-indirect activation of macrophages by photodynamically killed tumor cells. J. Photochem. Photobiol., 1999, Vol.50, №2-3, P.99-107.
- Roberts D.J., Cairnduff F. Photodynamic therapy ofprimary skin cancer: a review. Br. J. Surg., 1995, Vol. 48, №6, Р.360-370.
- Selman S.H., Kreimer-Birnbaum M., at all. Blood flow in transplantable bladder tumors treated with hematoporphyrin derivative and light. Cancer. Res., 1984,Vol. 44, №5, Р.1924-1927.
- Wieman T.J., Mang T.S., Fingar V.H., Hill T.G., Reed M.W., Corey T.S., Nguyen V.Q., Render E.R. Effect of photodynamic therapy on blood flow in normal and tumor vessels. Surgery, 1988, Vol.104, №3, P.512-517.

 +7(995)120-57-57
+7(995)120-57-57